金屬(shu)與腐(fu)蝕介(jie)質之間由于化學(xue)和(he)電化學(xue)作(zuo)用而引起的(de)損傷或失效。
一、按(an)腐蝕作用(yong)的(de)性質分類
可分為化(hua)學腐蝕和電化(hua)學腐蝕。
①. 化學(xue)腐蝕
在非電解質溶液中所產生的腐蝕,例如高溫下不銹(xiu)鋼的氧化(化學腐蝕不屬于本節討論范圍)。
②. 電化學腐蝕(shi)
鋼(gang)鐵和不銹鋼(gang)在(zai)潮濕大氣、水溶(rong)液和酸、堿、鹽等(deng)電解質(zhi)溶(rong)液中所產生的腐(fu)蝕(shi),在(zai)腐(fu)蝕(shi)過程中有離子(電子)產生。電化(hua)學(xue)腐(fu)蝕(shi)的實(shi)質(zhi)是(shi)原電池的作用。
在(zai)水溶液(ye)中(zhong)(zhong),前(qian)面已述(shu)及(ji)金(jin)屬(shu)(shu)變為(wei)離子(zi)(zi)(離子(zi)(zi)化(hua)),這就是腐蝕,而金(jin)屬(shu)(shu)離子(zi)(zi)化(hua)的(de)難易,即離子(zi)(zi)化(hua)的(de)傾向(xiang)則(ze)系以(yi)其標(biao)準(zhun)電(dian)(dian)(dian)(dian)極(ji)(ji)(ji)電(dian)(dian)(dian)(dian)位來表征,人們以(yi)氫(qing)(H+)的(de)標(biao)準(zhun)電(dian)(dian)(dian)(dian)極(ji)(ji)(ji)電(dian)(dian)(dian)(dian)位為(wei)基準(zhun),離子(zi)(zi)化(hua)傾向(xiang)較大,即標(biao)準(zhun)電(dian)(dian)(dian)(dian)極(ji)(ji)(ji)電(dian)(dian)(dian)(dian)位較負的(de)金(jin)屬(shu)(shu)為(wei)陽極(ji)(ji)(ji),而離子(zi)(zi)化(hua)傾向(xiang)較小,即標(biao)準(zhun)電(dian)(dian)(dian)(dian)極(ji)(ji)(ji)電(dian)(dian)(dian)(dian)位較正的(de)金(jin)屬(shu)(shu)為(wei)陰極(ji)(ji)(ji)。在(zai)水溶液(ye)中(zhong)(zhong),陰極(ji)(ji)(ji)與陽極(ji)(ji)(ji)間(jian)的(de)標(biao)準(zhun)電(dian)(dian)(dian)(dian)極(ji)(ji)(ji)電(dian)(dian)(dian)(dian)位之差是金(jin)屬(shu)(shu)電(dian)(dian)(dian)(dian)化(hua)學腐蝕的(de)動力(li)。
在鋼鐵和(he)不(bu)銹鋼等金屬(shu)電(dian)(dian)化學腐蝕(shi)的條件下,與原電(dian)(dian)池的不(bu)同點是陽極釋放(fang)電(dian)(dian)子的陽極過程和(he)陰(yin)極獲得(de)電(dian)(dian)子的陰(yin)極過程系在同一金屬(shu)的表面上進行的,由于此(ci)過程用肉眼不(bu)可見,人們將此(ci)種陽極-陰(yin)極構成的電(dian)(dian)池稱(cheng)為腐蝕(shi)微電(dian)(dian)池。
·鋼(gang)鐵生銹(xiu)的電化學腐(fu)蝕過程
鋼鐵在表(biao)面(mian)上有水和氧 存在的(de)(de)介質(zhi)中,基體中的(de)(de)鐵(Fe)會(hui)成為鐵離子,即 這就(jiu)是陽(yang)極氧化反(fan)應(ying);同時,溶液中的(de)(de)氧(接受了游離的(de)(de)電子(e)進行著陰極反(fan)應(ying),即,這是陰極還(huan)原反(fan)應(ying),經過: 和3就(jiu)是反(fan)應(ying)所形(xing)成的(de)(de)鐵銹。
如果鋼鐵是(shi)在酸性溶(rong)液中,因為H+濃度高(即(ji)pH值(zhi)低(di)),H+可接(jie)受(shou)電子(e)反應生(sheng)成,即(ji),這是(shi)鐵產生(sheng)了析出氫的腐蝕(shi)。
·不銹鋼的(de)電化學(xue)腐蝕過程和(he)陽極(ji)極(ji)化曲(qu)線(xian)
將不(bu)銹鋼或可鈍化(hua)的(de)金屬置于電(dian)解(jie)質溶(rong)液中,采用(yong)現代(dai)電(dian)化(hua)學(xue)技術測定(ding)電(dian)極(ji)電(dian)位(E)與(yu)腐(fu)蝕(shi)電(dian)流(i)間的(de)關系便可得到(dao)描(miao)述不(bu)銹鋼電(dian)化(hua)學(xue)腐(fu)蝕(shi)過程的(de)陽極(ji)極(ji)化(hua)曲(qu)線(示(shi)意圖(tu)(tu)見圖(tu)(tu)8.1。從(cong)此圖(tu)(tu)可看出典型的(de)陽極(ji)極(ji)化(hua)曲(qu)線系由活性溶(rong)解(jie)區(qu)(活化(hua)區(qu));鈍化(hua)過渡區(qu);鈍化(hua)(態)區(qu)和(he)過鈍化(hua)區(qu)(電(dian)位高于 等四(si)部分所組成。
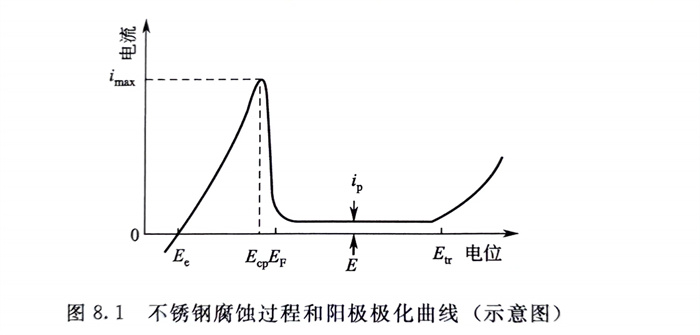
活化區 隨電位(wei)升(sheng)高,陽極(ji)溶解電流密度不斷(duan)增加,當為鈍化電位(wei)),陽極(ji)溶解電流密度達(da)到最大(da)值 ,此時不銹鋼(gang)的溶解處于(yu)活化腐蝕(shi)狀態(tai)。
鈍化過渡區(qu) 此區(qu)與 為活化電(dian)位)之(zhi)間相距(ju)很近,當(dang)溶解電(dian)流(liu)密度(du)越(yue)過最大(da)值(zhi)后,隨后急(ji)劇下降且處(chu)于不穩定態,此時,很難測得各點的穩定數值(zhi)。
鈍(dun)化(態(tai))區 電位高(gao)于EF時,不(bu)銹(xiu)鋼(gang)(gang)表面形成富鉻(ge)氧化物(鈍(dun)化膜),阻礙不(bu)銹(xiu)鋼(gang)(gang)的溶(rong)解(jie)的進行。此時陽極溶(rong)解(jie)電流密度(du)(稱維鈍(dun)電流)很小(僅約(yue)幾十萬分之(zhi)一),且基本與電位無關。在此區內,陽極溶(rong)解(jie)的腐(fu)蝕(shi)產物與活(huo)化溶(rong)解(jie)區活(huo)性溶(rong)解(jie)時的腐(fu)蝕(shi)產物完全不(bu)同(tong)。此時的氧化膜的腐(fu)蝕(shi)速率(lv)代表著此不(bu)銹(xiu)鋼(gang)(gang)的腐(fu)蝕(shi)速率(lv)。
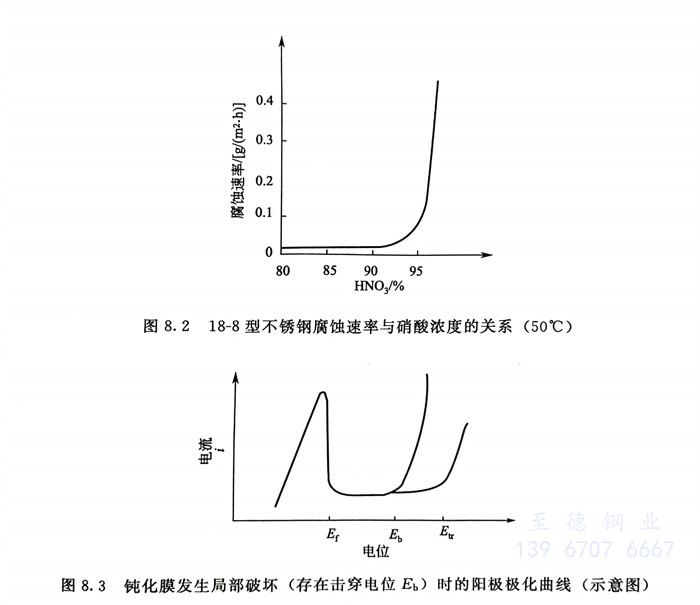
過(guo)鈍(dun)化(hua)(hua)區(qu) 電(dian)位(wei)超過(guo)后稱過(guo)鈍(dun)化(hua)(hua)電(dian)位(wei)),隨電(dian)位(wei)升高電(dian)流(liu)密度(du)再次增大,此時有的(de)(de)(de)不銹(xiu)鋼,例(li)如18-8(304)在(zai)硝(xiao)酸中(zhong)當酸濃(nong)度(du)達到高濃(nong)條件時,會由(you)于鈍(dun)化(hua)(hua)膜(mo)的(de)(de)(de)三(san)價(jia)鉻離子(zi)(zi)氧(yang)化(hua)(hua)成六價(jia)鉻離子(zi)(zi)(而受(shou)到破壞,使不銹(xiu)鋼溶解速(su)度(du)上(shang)升,出現腐蝕速(su)率上(shang)升的(de)(de)(de)全(quan)面(mian)腐蝕(見圖(tu)(tu)8.2)。從圖(tu)(tu)8.2可知,在(zai)50℃條件下當硝(xiao)酸濃(nong)度(du)大于90%時,18-8鋼的(de)(de)(de)腐蝕速(su)率開始(shi)急劇增加,即在(zai)此溫(wen)度(du)下,18-8鋼出現過(guo)鈍(dun)化(hua)(hua)腐蝕的(de)(de)(de)臨界(jie)硝(xiao)酸濃(nong)度(du)應為90%。
圖(tu)8.3指出,當不銹鋼的(de)(de)電(dian)極電(dian)位未達到過(guo)鈍(dun)化電(dian)位前,而達到Eb 電(dian)位時(shi),不銹鋼的(de)(de)腐(fu)(fu)蝕(shi)(shi)電(dian)流(liu)密度也(ye)急劇上(shang)升,這(zhe)表(biao)明(ming)不銹鋼有局部腐(fu)(fu)蝕(shi)(shi)-點蝕(shi)(shi)(孔蝕(shi)(shi))出現(xian),Eb則稱為點蝕(shi)(shi)(孔蝕(shi)(shi))電(dian)位或擊穿電(dian)位。這(zhe)種腐(fu)(fu)蝕(shi)(shi)現(xian)象極易在(zai)(zai)含(han)有Cl-等活性(xing)離子的(de)(de)介質中出現(xian),這(zhe)與(yu)在(zai)(zai)鈍(dun)化膜薄弱部位Cl-的(de)(de)存在(zai)(zai)會與(yu)氧(yang)(O)和氫氧(yang)根(OH)進(jin)行置換形(xing)成金屬氧(yang)化物的(de)(de)鉻鹽所(suo)導致的(de)(de)鈍(dun)化膜結構的(de)(de)破壞有關。
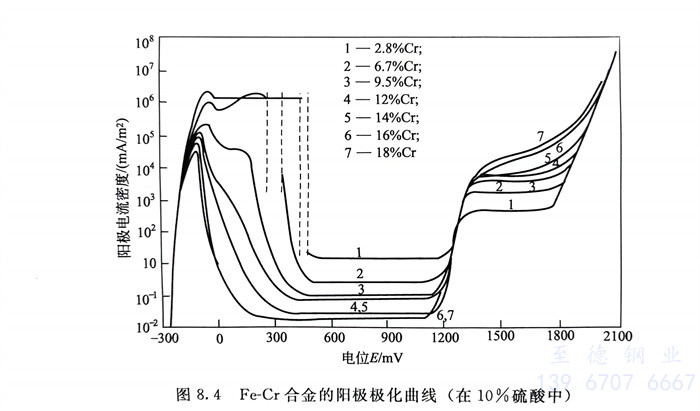
從研(yan)究(jiu)一些因素(su)對(dui)不(bu)銹(xiu)鋼(gang)陽(yang)極極化(hua)(hua)(hua)行為的(de)(de)影(ying)響中(zhong)發(fa)現,凡有利于(yu)(yu)下述(shu)因素(su)的(de)(de)變化(hua)(hua)(hua),均(jun)對(dui)不(bu)銹(xiu)鋼(gang)的(de)(de)鈍(dun)化(hua)(hua)(hua)有益。例如(ru),能使(shi)最大鈍(dun)化(hua)(hua)(hua)電(dian)(dian)流imax減小(xiao),鈍(dun)化(hua)(hua)(hua)起始電(dian)(dian)位和鈍(dun)化(hua)(hua)(hua)終止電(dian)(dian)位向(xiang)負向(xiang)移動(dong)(dong),不(bu)銹(xiu)鋼(gang)就(jiu)變得易于(yu)(yu)鈍(dun)化(hua)(hua)(hua);當(dang)鈍(dun)化(hua)(hua)(hua)膜的(de)(de)擊穿電(dian)(dian)位和過鈍(dun)化(hua)(hua)(hua)電(dian)(dian)位 朝(chao)正向(xiang)移動(dong)(dong)時(shi)(shi)(shi),穩定鈍(dun)化(hua)(hua)(hua)區將擴(kuo)大,鈍(dun)態(tai)腐蝕(shi)(shi)(shi)電(dian)(dian)流密度(du)將減小(xiao),這會有利于(yu)(yu)提高(gao)鈍(dun)化(hua)(hua)(hua)的(de)(de)完善程(cheng)度(du),降低(di)鈍(dun)態(tai)的(de)(de)腐蝕(shi)(shi)(shi)速度(du)。圖8.4系在中(zhong), 合(he)金(jin)的(de)(de)陽(yang)極極化(hua)(hua)(hua)曲(qu)線。可以看(kan)出鋼(gang)中(zhong)鉻量(liang)對(dui)其陽(yang)極極化(hua)(hua)(hua)曲(qu)線的(de)(de)影(ying)響以及 后,此不(bu)銹(xiu)鋼(gang)易于(yu)(yu)從活化(hua)(hua)(hua)態(tai)向(xiang)鈍(dun)態(tai)轉變的(de)(de)趨向(xiang)。同時(shi)(shi)(shi),此圖還指出了即使(shi)合(he)金(jin)中(zhong)含≥12%Cr已處(chu)于(yu)(yu)穩定鈍(dun)化(hua)(hua)(hua)態(tai)時(shi)(shi)(shi),其腐蝕(shi)(shi)(shi)電(dian)(dian)流密度(du)雖然很(hen)小(xiao),但并不(bu)是(shi)零(ling)。這就(jiu)告訴我(wo)們,處(chu)于(yu)(yu)鈍(dun)態(tai)的(de)(de)合(he)金(jin)耐腐蝕(shi)(shi)(shi)但這并不(bu)是(shi)不(bu)腐蝕(shi)(shi)(shi)。
二(er)、按(an)腐蝕(shi)的形態分類
可分為全(quan)面(均(jun)勻)腐(fu)蝕和(he)局部腐(fu)蝕。
全(quan)面腐(fu)蝕:腐(fu)蝕分布在介質與不銹(xiu)鋼相接觸的(de)整個界面上,全(quan)面腐(fu)蝕主要出現在酸、堿、鹽等腐(fu)蝕環境(jing)中;
局部腐蝕:腐蝕分布在不銹鋼表面的某些局部。局部腐蝕多出現在含鹵素離子,例如Cl-的大氣和水環境中。
局(ju)部腐(fu)蝕的(de)危害遠遠大(da)于(yu)全面(mian)腐(fu)蝕,許多局(ju)部腐(fu)蝕常(chang)常(chang)在設備、構件等沒有(you)任(ren)何(he)宏(hong)觀變(bian)形(xing)甚(shen)至在沒有(you)任(ren)何(he)破損(sun)預兆的(de)情況下,就會(hui)迅速、突然地破壞,從而造成嚴重的(de)甚(shen)至是災難性的(de)后果。



