三氯化鐵溶液作為不銹鋼的化學腐蝕加工的腐蝕劑的優點如下。
①. 特別適用于用明膠、骨膠與重鉻酸鹽感光劑作抗蝕劑的情況。三氯化鐵不屬于強酸、強堿之列,對上述抗蝕劑的腐蝕極微小,提高了不銹鋼腐(fu)蝕加工的合格率。
②. 用波美相(xiang)對密(mi)度計(ji)控制和檢測濃(nong)度方便。輔用電子(zi)毫伏計(ji)、鉑電極(ji)和飽和甘汞電極(ji)測量電位,能夠(gou)準確地控制腐蝕(shi)速(su)率。
③. 可使(shi)用鈦泵(beng)作為(wei)循(xun)環壓力泵(beng),提高腐(fu)蝕(shi)速率。金屬(shu)鈦對三氯化鐵是較穩定的(de)。
④. 腐蝕液(ye)氧化還原(yuan)電位降低后,可以使(shi)廢液(ye)再生,能將廢液(ye)的(de)氧化還原(yuan)電位復升至原(yuan)液(ye)水(shui)平,降低了(le)成本,避免了(le)環境污染。
一、三氯化鐵溶(rong)液腐蝕機(ji)理(li)
三氯化鐵腐蝕不(bu)銹鋼(如1Cr18Ni9)的(de)主要氧化還(huan)原(yuan)反應如下。
鐵(tie)(tie)與三氯化鐵(tie)(tie)反應生成二氯化鐵(tie)(tie): Fe+2FeCl3=3FeCl2
鉻(ge)與(yu)三氯(lv)化鐵(tie)反應生成三氯(lv)化鉻(ge)和(he)二氯(lv)化鐵(tie): Cr+3FeCl3=CrCl3+3FeCl2
鎳(nie)與三氯(lv)(lv)(lv)化(hua)鐵反應生成二氯(lv)(lv)(lv)化(hua)鎳(nie)和二氯(lv)(lv)(lv)化(hua)鐵:Ni+2FeCl3=NiCl2+2FeCl2
在25℃時的(de)標(biao)準電位查得:
φ(Fe3+/Fe2+)=0.771V
φ(Fe2+/Fe)=-0.44V
φ(Cr3+/Cr)=-0.74V
φ(Ni2+/Ni)=-0.25V
隨著腐蝕過程的進行,體系內三價鐵(Fe3+)減少,二價鐵(Fe2+)、二價鎳(Ni2+)及三價鉻(Cr3+)增加,體系氧化還原電位變負,腐蝕速率下降是腐蝕反應的必然趨勢。
二(er)、工藝參數(shu)
最佳腐蝕工藝配方的確定:通過氧化-還原電位的測定、波美相對密度的測定,不銹鋼腐蝕過程重量變化的精確量度,找出腐蝕規律,求得最佳腐蝕工藝配方及始終點。腐蝕液初始濃度:三氯化鐵溶液42°Bé;初始氧化還原電位560mV以上;腐蝕液氧化-還原電位降至480mV以下,加雙氧水(H2O2)與鹽酸(HCI)混合液將電位提升至540~560mV。
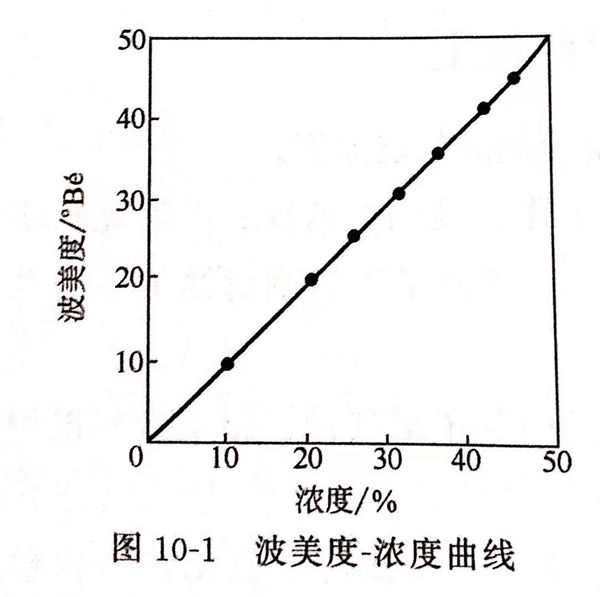
1. 波(bo)美相對密度(du)與三氯化鐵溶液百(bai)分濃度(du)的(de)關系(xi)圖(tu)
見圖 10-1,在操作(zuo)溫度30℃時測得。此圖可用作(zuo)濃度-波(bo)美度換(huan)算曲(qu)線。
2. 不同濃度的氧化還(huan)原(yuan)電位
用PHS-2C型(xing)酸度計或(huo)PZ-26b型(xing)數字電(dian)壓表,用光(guang)滑鉑(bo)電(dian)極(ji)為(wei)正(zheng)極(ji),飽和甘汞電(dian)極(ji)(SCE)為(wei)負極(ji),測量溶(rong)液的氧化(hua)還原電(dian)位,氧化(hua)還原電(dian)位值均為(wei)相對(dui)于SCE電(dian)位值,溫度30℃,用化(hua)學純或(huo)工業級(ji)三氯(lv)化(hua)鐵(FeCl3)配制溶(rong)液,其結(jie)果見表10-1。
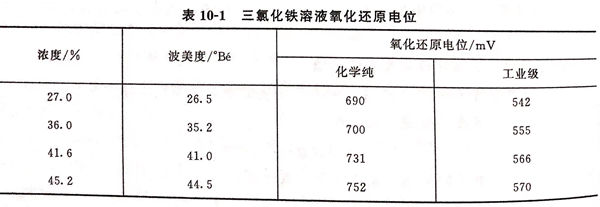
由表10-1可見:隨著(zhu)溶(rong)液(ye)濃(nong)度的增加,氧化(hua)還原(yuan)電位(wei)變正(zheng)。對于一定等級一定濃(nong)度的三(san)氯(lv)化(hua)鐵(tie)溶(rong)液(ye),其氧化(hua)還原(yuan)電位(wei)基本上應為一定值,如果(guo)電位(wei)值偏(pian)負,意味著(zhu)部分三(san)氯(lv)化(hua)鐵(tie)被還原(yuan)。工業(ye)級三(san)氯(lv)化(hua)鐵(tie)因純度不高,氧化(hua)還原(yuan)電位(wei)較(jiao)負,42°Bé工業(ye)級三(san)氯(lv)化(hua)鐵(tie)的氧化(hua)還原(yuan)電位(wei)一般應比(bi)(bi)560mV正(zheng)。否則(ze),應加過氧化(hua)氫及鹽酸(suan)混合液(ye),將電位(wei)調到比(bi)(bi)560mV正(zheng)。
3. 腐(fu)蝕過程中腐(fu)蝕液氧化還原電位與腐(fu)蝕速率的關系
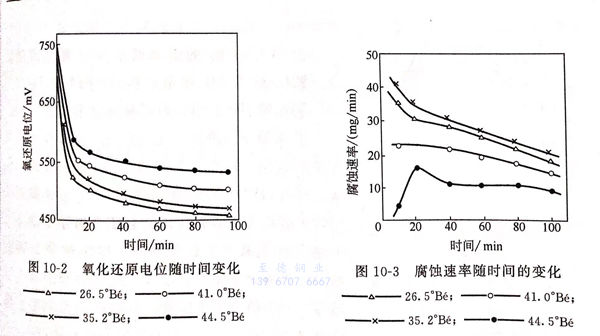
腐(fu)蝕(shi)過程(cheng)中三氯(lv)化鐵溶液氧化還(huan)原電位隨時間的(de)(de)變化見圖(tu)10-2.由圖(tu)10-2可見,不論溶液濃度多大、初始氧化還(huan)原電位值多正,隨著腐(fu)蝕(shi)的(de)(de)進(jin)行,電位都是下降的(de)(de)。腐(fu)蝕(shi)開始的(de)(de)10min內,電位很快(kuai)下降170mV左(zuo)右,以后的(de)(de)變化趨勢逐漸減少(shao)。
4. 腐蝕速率隨(sui)腐蝕時間的變化
不(bu)同(tong)濃(nong)(nong)(nong)度(du)(du)的(de)三氯化鐵溶(rong)液中腐(fu)蝕(shi)(shi)(shi)(shi)(shi)速(su)率(lv)隨腐(fu)蝕(shi)(shi)(shi)(shi)(shi)時間的(de)變化見圖(tu)(tu)10-3.由圖(tu)(tu)10-3可見,隨著腐(fu)蝕(shi)(shi)(shi)(shi)(shi)時間的(de)增長,腐(fu)蝕(shi)(shi)(shi)(shi)(shi)速(su)率(lv)大致趨勢是降低的(de)。聯系(xi)圖(tu)(tu)10-2氧(yang)化還原電(dian)位(wei)(wei)隨腐(fu)蝕(shi)(shi)(shi)(shi)(shi)時間變得(de)越(yue)(yue)來越(yue)(yue)負的(de)規律,很容(rong)易得(de)到同(tong)一濃(nong)(nong)(nong)度(du)(du)下,氧(yang)化還原電(dian)位(wei)(wei)越(yue)(yue)正(zheng),腐(fu)蝕(shi)(shi)(shi)(shi)(shi)速(su)率(lv)越(yue)(yue)大的(de)結論。也就是說,濃(nong)(nong)(nong)度(du)(du)相同(tong),氧(yang)化還原電(dian)位(wei)(wei)不(bu)同(tong),腐(fu)蝕(shi)(shi)(shi)(shi)(shi)速(su)率(lv)也不(bu)同(tong),電(dian)位(wei)(wei)值(zhi)越(yue)(yue)負,腐(fu)蝕(shi)(shi)(shi)(shi)(shi)速(su)率(lv)越(yue)(yue)慢。
5. 工(gong)業級和化學純三氯(lv)化鐵溶(rong)液的腐(fu)蝕速率比較
用工業(ye)級和化(hua)學純三氯(lv)化(hua)分別配成37°Bé的三氯(lv)化(hua)鐵溶液的電位以及腐蝕速率見表10-2。
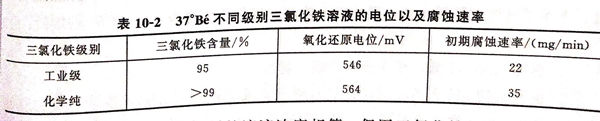
由(you)表10-2可見,雖(sui)然配制的(de)溶液濃度相等,但因三(san)氯化(hua)鐵的(de)有(you)效含量不同,化(hua)學純的(de)氧(yang)化(hua)還(huan)原電位值(zhi)比工業級的(de)電位值(zhi)正,其腐(fu)蝕速率較工業級的(de)大。
三、影響(xiang)腐蝕速(su)率的因素
1. 腐蝕(shi)液濃度對(dui)腐蝕(shi)速率的影響
4 種不同濃(nong)度(du)腐(fu)蝕(shi)(shi)液(ye)腐(fu)蝕(shi)(shi)304不銹(xiu)鋼時,腐(fu)蝕(shi)(shi)量隨(sui)時間的變化見圖10-4。由圖10-4可(ke)見,35.2°Bé線(xian)(xian)位居各(ge)線(xian)(xian)之(zhi)上,44.5°Bé線(xian)(xian)位居各(ge)線(xian)(xian)之(zhi)下,26.5°Bé線(xian)(xian)僅次于35.2°Bé線(xian)(xian),41°Bé線(xian)(xian)居中。也就是(shi)說(shuo),腐(fu)蝕(shi)(shi)液(ye)濃(nong)度(du)太(tai)高或(huo)太(tai)低(di)時,都不能獲得(de)最大腐(fu)蝕(shi)(shi)速(su)率(lv)。只有在適當的濃(nong)度(du)區間才可(ke)能獲得(de)理(li)想的腐(fu)蝕(shi)(shi)速(su)率(lv)。
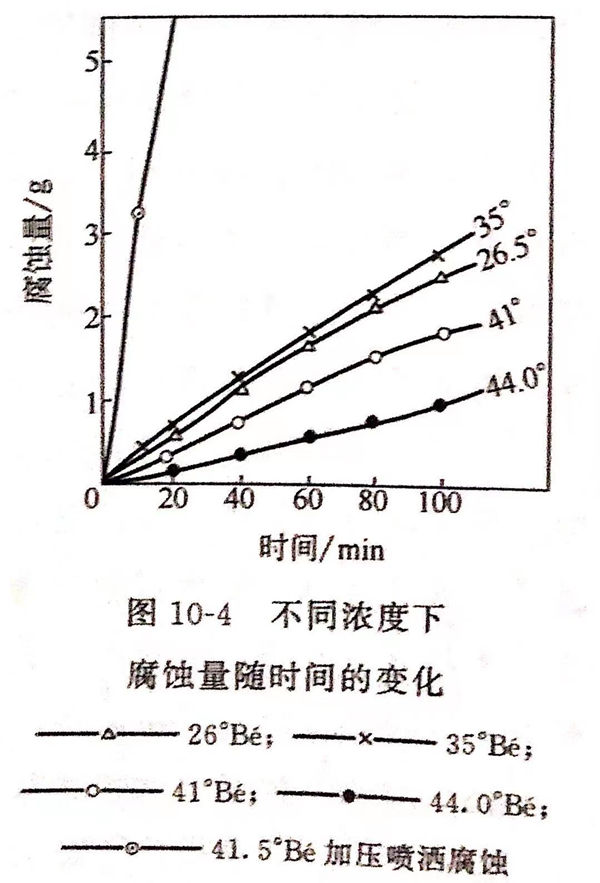
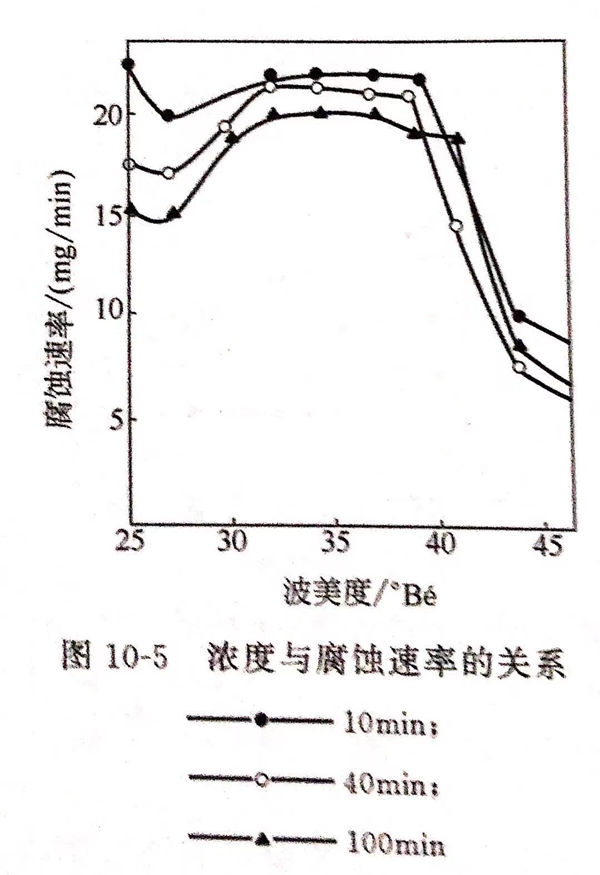
為(wei)了(le)找到(dao)這一濃(nong)度(du)區間,采用(yong)各(ge)種濃(nong)度(du)溶液在不同腐蝕(shi)(shi)時間測得的腐蝕(shi)(shi)速率(lv)見圖(tu)10-5,由圖(tu)可得出以(yi)下結(jie)論。
①. 在31~39°Bé的(de)腐蝕(shi)液中,腐蝕(shi)速率較(jiao)大。
②. 小于31°Bé的腐蝕液中含三氯化鐵量較少,氧化還原電位較負,腐蝕過程中Fe3+與Fe2+的比值下降迅速,因而腐蝕速率較低。
③. 溶液相對密度大于40°Bé,雖有較正的氧化還原電位,Fe3+、Fe2+的比例降低較慢,但從金屬表面腐蝕下來的Fe2+、Cr3+等金屬離子很難擴散離開金屬表面,從而使金屬原子溶解下來變為相應離子的趨勢變小,腐蝕速率顯著下降。從熱力學角度看,有較大的腐蝕潛力和反應趨勢,但從動力學度看,濃度過高反而降低腐蝕速率。
④. 在生(sheng)(sheng)產中(zhong)既(ji)要考(kao)慮腐(fu)蝕速率以(yi)提高(gao)生(sheng)(sheng)產效率,又(you)要考(kao)慮腐(fu)蝕質(zhi)量(liang)和廢液(ye)再生(sheng)(sheng)的要求,以(yi)保證產品質(zhi)量(liang)及腐(fu)蝕液(ye)多次循環再生(sheng)(sheng),不至于使(shi)(shi)濃(nong)度降得太低,腐(fu)蝕機上使(shi)(shi)用三氯化鐵濃(nong)度為40~42°Bé的溶液(ye)。
2. 腐(fu)蝕液的(de)pH的(de)影響
①. 腐蝕(shi)(shi)液的(de)pH低,有利于不銹鋼的(de)腐蝕(shi)(shi)。
②. 腐蝕液的pH太高,三氯化鐵水解成氫氧化鐵[Fe(OH)3]沉淀,失去腐蝕作用。在生產中,腐蝕液用到一定程度要適當加入一些鹽酸。
3. 腐蝕液溫(wen)度的影響
溫度(du)(du)越高,腐(fu)蝕(shi)速率越大。但(dan)考(kao)慮到抗蝕(shi)膜的(de)承受能力,一般可用30~40℃的(de)溫度(du)(du)。
4. 腐(fu)蝕方式及液壓對(dui)腐(fu)蝕速率(lv)的影響
2kg液壓的噴射腐(fu)(fu)(fu)蝕(shi)(shi),將腐(fu)(fu)(fu)蝕(shi)(shi)時(shi)間由(you)原(yuan)來(lai)靜態腐(fu)(fu)(fu)蝕(shi)(shi)的60min減少至動態腐(fu)(fu)(fu)蝕(shi)(shi)的6min。由(you)于動態腐(fu)(fu)(fu)蝕(shi)(shi),使腐(fu)(fu)(fu)蝕(shi)(shi)產物盡(jin)快離開(kai)不銹鋼表面,讓盡(jin)量(liang)多的三價鐵與(yu)(yu)金屬(shu)表面動能(neng)撞擊,提(ti)高反應速率。由(you)于被腐(fu)(fu)(fu)蝕(shi)(shi)工件與(yu)(yu)腐(fu)(fu)(fu)蝕(shi)(shi)液的滯留(liu)時(shi)間只有靜態時(shi)間的1/10,在(zai)抗(kang)蝕(shi)(shi)膜破壞前(qian)腐(fu)(fu)(fu)蝕(shi)(shi)已經完(wan)成(cheng),因而腐(fu)(fu)(fu)蝕(shi)(shi)質量(liang)提(ti)高,成(cheng)品率由(you)40%提(ti)高到95%以上。
5. 不銹(xiu)鋼表面鈍化膜的影響(xiang)
在(zai)靜態腐(fu)(fu)蝕(shi)(shi)中,腐(fu)(fu)蝕(shi)(shi)液(ye)(ye)的(de)濃(nong)度低于(yu)38°Bé,腐(fu)(fu)蝕(shi)(shi)速率很快(kuai)時,不銹鋼表面蒙有(you)一層(ceng)黑色(se)膠狀金屬(shu)沉(chen)積膜(mo),在(zai)30~38°Bé間,濃(nong)度越低,膜(mo)層(ceng)越厚,腐(fu)(fu)蝕(shi)(shi)減(jian)速嚴重。用等離子光量計分析(xi),殘渣(zha)中鐵(tie)、鉻(ge)、硫、鈣、硅(gui)的(de)相(xiang)對含量較高,可能存在(zai)硫化鐵(tie)、硫化鉻(ge)、硅(gui)酸鈣,都較難溶于(yu)三(san)氯(lv)化鐵(tie)腐(fu)(fu)蝕(shi)(shi)液(ye)(ye)中,加(jia)酸可以將其(qi)溶解,在(zai)加(jia)壓噴灑腐(fu)(fu)蝕(shi)(shi)中可將其(qi)從(cong)不銹鋼表面排(pai)除。
四、廢舊腐蝕液的再生
1. 腐蝕液的老化(hua)
隨著腐蝕過程的進行,體系氧化態Fe3+濃度下降,還原態Fe2+濃度增高,腐蝕液氧化還原電位降低。與此同時,溶液總金屬離子濃度不斷上升,最后導致腐蝕液失去腐蝕能力。
2. 腐蝕液的再生
加過氧化氫(H2O2)和鹽酸混合液,能將廢液氧化還原電位復升至原液水平,即提升至540~560mV。



